Здоровье кишечника зависит от разных факторов, в частности от кормления, а также от микробиологических, иммунологических и физиологических особенностей организма. При ухудшении здоровья желудочно-кишечного тракта нарушаются переваривание и усвоение питательных веществ, снижается коэффициент конверсии корма и повышается восприимчивость животных и птицы к заболеваниям. Все это в конечном итоге приводит к экономическим потерям.
Здоровый кишечник
Целостное сообщество микроорганизмов кишечника называют микробиомом. В него входят разнообразные популяции бактерий, грибов, простейших и вирусов. Состав микробиома в разных отделах желудочно-кишечного тракта различается. Это объясняется тем, что в одних отделах кишечника условия для микробных сообществ менее благоприятны, в других, наоборот, способствуют росту микроорганизмов.
Микробиом желудочно-кишечного тракта играет важную роль в пищеварительной, физиологической и иммунной системах. Ухудшение здоровья кишечника связано с чрезмерной его колонизацией патогенами и восприимчивостью к инфекционным заболеваниям, что может стать причиной снижения скорости роста сельскохозяйственных животных и птицы и повышения уровня падежа.
Формирование микробиоты зрелого кишечника начинается с момента вывода цыплят или рождения животных и зависит от многих факторов, в том числе от вида животного, типа кормления и применяемой в хозяйстве технологии.
Микробы поступают в кишечник преимущественно с кормом и водой. Поскольку персонал на фермах тоже может быть источником заражения, необходимо принимать меры, чтобы своевременно предотвратить занос на предприятие патогенных микроорганизмов.
В желудочно-кишечном тракте происходит взаимодействие между микробными клетками и компонентами корма. Следовательно, общее физиологическое состояние организма зависит от состава микробиоты кишечника. Однако точный механизм влияния последней на макроорганизм досконально не изучен.
Разнообразие микробиома играет важную роль. Полезные микроорганизмы создают защитный барьер внутри кишечника, что препятствует росту патогенных бактерий рода Salmonella, Campylobacter, Clostridium и Escherichia.
Существует много версий того, каким образом полезные микробы предотвращают колонизацию ЖКТ болезнетворными бактериями. Согласно одним теориям, полезные микробы занимают места прикрепления к клеткам, тем самым снижая вероятность прикрепления к ним патогенов и риск последующей колонизации кишечника. Приверженцы других теорий считают, что микробиота кишечника синтезирует различные вещества, например летучие жирные кислоты, органические кислоты и природные антимикробные элементы, которые либо подавляют рост нежелательных бактерий, либо делают среду их обитания менее благоприятной.
В опытах на стерильных животных было продемонстрировано, что кишечная микрофлора необходима для развития, созревания и стимуляции иммунной системы. Кроме того, микробиом кишечника может оказывать влияние на скорость роста хозяина за счет дополнительного производства питательных веществ (они образуются при расщеплении трудноперевариваемых компонентов корма).
Знания о роли микробных сообществ кишечника дают возможность более подробно изучить механизм действия существующих кормовых добавок и на основании полученных данных создавать новые продукты. Их ввод в рационы для животных и птицы позволит повысить продуктивность, улучшить здоровье и нормализовать общее состояние поголовья.
Кормовые добавки, применяемые с целью восстановления микробного разнообразия в кишечнике и снижения восприимчивости животного к заболеваниям, классифицируют как пребиотики и пробиотики. Благодаря появлению молекулярных методов исследований удалось преодолеть трудности, обусловленные сложностью культивирования кишечных бактерий. Это позволило достичь значительного прогресса в понимании того, какое влияние на состав микробиома оказывают разнообразные алиментарные факторы.
В последние годы исследователи особое внимание уделяли изучению влияния пребиотических препаратов на основе клеточных стенок дрожжей, в частности богатой маннанами фракции (БМФ), на популяции микробов.
Восстановление микробиома
Существует большое количество кормовых добавок, применение которых способствует стабилизации кишечной микрофлоры, улучшению здоровья ЖКТ и снижению восприимчивости животного к заболеваниям. К таким продуктам относят вакцины против кокцидиоза, пробиотики, препараты, в основе действия которых лежит механизм конкурентного исключения, кормовые ферменты, функциональные питательные вещества (нуклеотиды), органические кислоты, средства, поддерживающие гигиену корма на высоком уровне, органические минералы, фитобиотики и пребиотики (в частности, богатую маннанами фракцию клеточных стенок дрожжей).
Одно из эффективных средств, использующихся сегодня в кормлении животных для восстановления кишечной микрофлоры, — БМФ, получаемая из клеточных стенок дрожжей. БМФ и антибиотики — стимуляторы роста обладают одинаковыми свойствами. Это подтвердили результаты экспериментов.
Продукты на основе БМФ появились на рынке в начале 1990‑х гг. С 1999 г. БМФ стали широко применять в кормлении животных. Это было связано с тем, что в странах Евросоюза ввели запрет на использование антибиотиков — стимуляторов роста.
Большинство кормовых добавок на основе БМФ производят из клеточных стенок дрожжей Saccharomyces cerevisiae. БМФ может связывать патогены и тем самым предотвращать колонизациию ими кишечника. Ввод в рационы продуктов на основе БМФ — эффективное решение, позволяющее отказаться от использования антибиотиков — стимуляторов роста.
Влияние БМФ на здоровье животных тщательно изучили и доказали ее эффективность. Отмечено, что при вводе БМФ в рационы оптимизировались такие параметры, как скорость роста и конверсия корма. Подтверждено, что использование продуктов с БМФ играет ключевую роль в профилактике колонизации кишечника патогенными микроорганизмами.
Новые исследования направлены на изучение влияния кормовой добавки на основе БМФ на микробиом кишечника птицы в целом, а не на конкретные виды бактерий — полезные или патогенные (Corrigan et al., 2015). Так, результаты анализа, выполненного по методу глубокого секвенирования, показали, что БМФ изменяет микробные популяции на разных филогенетических уровнях.
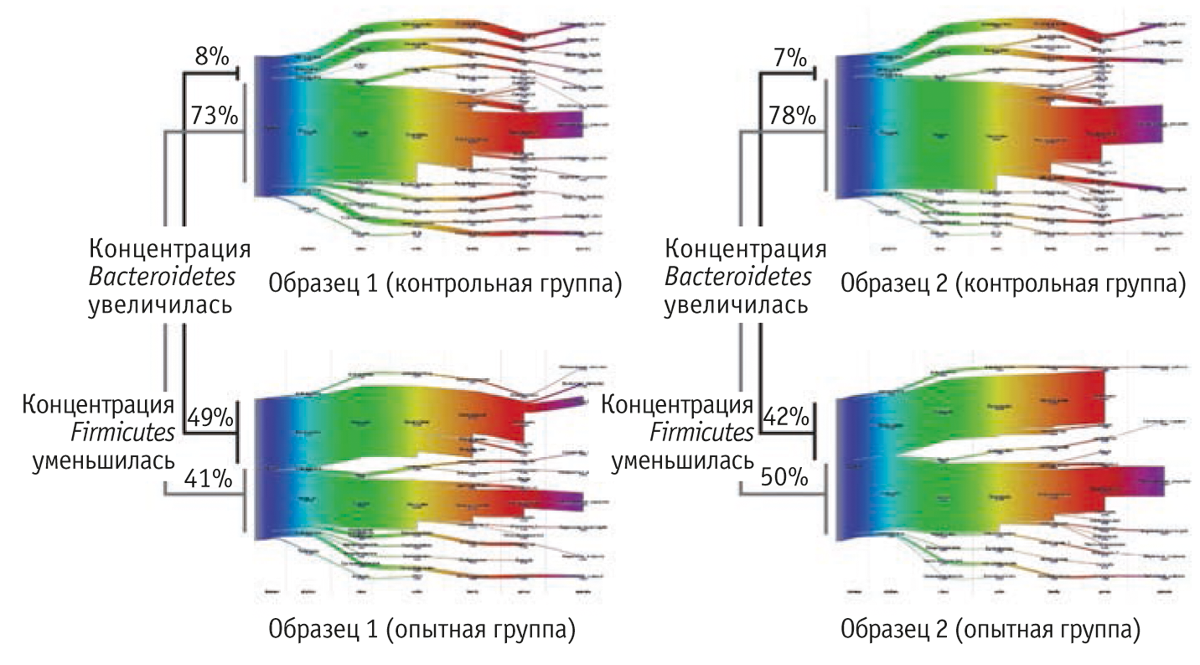
В рамках одного из исследований Corrigan и Murphy (2016) провели серию производственных опытов на бройлерах и установили, что при применении БМФ доля Bacteroidetes в составе микробиоты слепой кишки птицы увеличилась, а Firmicutes — уменьшилась (рисунок). Также было зафиксировано снижение концентрации бактерий группы Proteobacteria, к которой принадлежат такие патогены, как Escherichia и Salmonella.
В научной литературе есть данные о том, что улучшение разнообразия микробиома кишечника обусловлено его повышенной устойчивостью к колонизации патогенами. В ходе дополнительных исследований выявили, что БМФ обладает способностью увеличивать микробное разнообразие в слепой кишке бройлеров и снижать в ней уровень Campylobacter — патогена, представляющего опасность для человека (Corrigan and Murphy, 2016).
Применение кормовых добавок на основе богатой маннанами фракции клеточных стенок дрожжей позволяет оптимизировать состав микрофлоры ЖКТ за счет увеличения ее общего разнообразия, снижения патогенной нагрузки на кишечник и повышения его устойчивости к колонизации патогенами.
Результаты исследований наглядно продемонстрировали, что между кормлением и общим физиологическим состоянием птицы существует прямая зависимость. Следовательно, контроль распространения патогенов на птицефабриках играет ключевую роль: качество мяса и яйца влияет на здоровье конечного потребителя продукции птицеводства — человека.
Устойчивость к антимикробным веществам
Резистентность к антибиотикам может стать одной из величайших проблем для нынешнего поколения, ведь количество штаммов бактерий, невосприимчивых к существующим препаратам, постоянно увеличивается. Согласно статистическим данным, в США от болезней, вызываемых устойчивыми к антибиотикам бактериями, ежегодно умирают около 23 тыс. человек. Специалисты обеспокоены тем, что с 1998 г. Управление по контролю за продуктами питания и лекарственными средствами США (FDA) одобрило только два новых класса антибиотиков (основная часть применяемых сегодня средств была разработана до 1970‑х гг.).
Применение в ветеринарии противомикробных веществ, использующихся для лечения людей, а также препаратов из того же семейства или класса может привести к селекции устойчивых к ним зоонозных патогенов (например, Salmonella и Campylobacter). Человек заражается при контакте с животными или через продукты питания и воду.
Резистентные болезнетворные бактерии представляют собой часть крупной невосприимчивой к антимикробным веществам экосистемы. Установлено, что гены резистентности передаются от одних микроорганизмов другим, однако механизм такой передачи досконально еще не изучен.
В продукты питания патогены (в частности, Salmonella, Campylobacter и E. сoli) попадают при убое, переработке сырья и изготовлении продукции. Результаты последних исследований показали, что появились устойчивые к антимикробным веществам энтерококки, а кроме того, было подтверждено, что они передаются от животных работающим на ферме людям. В ходе этих исследований обнаружили идентичные или близкородственные подтипы бактерий в организме животных, человека и в продуктах питания, что подтверждает гипотезу об алиментарном пути передачи резистентности к антибиотикам.
В мире проблема безопасности продуктов питания с каждым годом становится все более актуальной, а значит, растет спрос на мясо, получаемое только от выращенных без использования кормовых антибиотиков животных и птицы. По этой причине возникла потребность в поиске альтернативы антибиотикам — стимуляторам роста.
Общепризнано, что волшебной таблетки, способной заменить антибиотики в животноводстве, не существует, и производителям, решившим отказаться от использования антибиотиков, придется приложить немало усилий, чтобы обеспечить оптимальные санитарно-гигиенические условия на фермах и комплексах.
Антибиотики оказывают неспецифическое действие на микробиом кишечника, в результате чего в ЖКТ снижается общее микробное разнообразие (Vrieze et al., 2014). Длительное применение антибиотиков может привести к возникновению и размножению резистентных видов бактерий за счет вытеснения не имеющих устойчивости симбиотических штаммов.
Одна из стратегий борьбы с отрицательными последствиями применения антибиотиков — восстановление микробного разнообразия в ЖКТ животных и птицы путем скармливания рационов, обогащенных БМФ.
Микробиом и метаболизм
Определение профиля микробов в кишечнике дает общее представление о составе его микрофлоры. Разработанные в последние годы сложные методы анализа позволяют оценить функциональные способности микробиома. Так, было установлено, что при добавлении в корм БМФ выравнивается соотношение между бактериями типа Bacteroidetes и Firmicutes (Corrigan et al., 2015). Сегодня появилась возможность определять, как питательные вещества влияют на состав микрофлоры кишечника, а в конечном итоге — на пищеварение и метаболизм.
Выводы
Доказано, что использование кормовых добавок на основе БМФ положительно влияет на бактериальное сообщество в целом. Изменяя общее микробное разнообразие в ЖКТ, можно восстановить его микрофлору. Такой прием позволяет уменьшить патогенную нагрузку на кишечник, повысить его устойчивость к колонизации болезнетворными микробами и снизить число резистентных к антибиотикам штамов.
ООО «Оллтек»
105062, Москва, Подсосенский пер., д. 26, стр. 3
Тел.: +7 (495) 258‑25‑25
E-mail: russia@alltech.com
www.alltech.com/russia


















